Wasserstoffverbrennung zur Dekarbonisierung von (Hochtemperatur)-Prozesswärme
Abstract
Der Klimawandel und die Dekarbonisierung stellen für energieintensive Industrien eine besondere Herausforderung dar. Energie wird in vielen Industrien vor allem als Prozesswärme auf sehr unterschiedlichen Temperaturniveaus für eine Vielzahl von hochgradig spezialisierten Fertigungsprozessen benötigt, mit hohen Anforderungen an Produktqualität, Wirtschaftlichkeit und Umweltverträglichkeit. Wasserstoff aus erneuerbaren Quellen stellt eine vielversprechende Option dar, diese Prozesse zu dekarbonisieren, bringt aber auch aufgrund seiner Verbrennungseigenschaften einige Besonderheiten mit sich, die bei diesen komplexen Anwendungen berücksichtigt werden müssen.
Einleitung
Der Klimawandel und die damit verbundene Notwendigkeit, anthropogene Treibhausgasemissionen (THG) zu minimieren, stellt eine globale Herausforderung dieses Jahrhunderts dar. Im Fokus liegen hier insbesondere die Emissionen, die mit der Bereitstellung von Energie verbunden sind, von der Stromerzeugung in Kraftwerken über Antriebsleistung für Fahrzeuge bis hin zur Wärme im häuslichen Sektor, aber auch in vielen Grundstoffindustrien. Die Prozesswärme ist für etwa 2/3 des industriellen Energiebedarfs in Deutschland verantwortlich [1] bzw. für etwa 18 % der deutschen THG-Emissionen [2].
Der weitaus überwiegende Teil des Prozesswärmebedarfs in Deutschland wird heute durch fossile Energieträger, vor allem Erdgas (ca. 45 %), gedeckt, während Strom oder erneuerbare Energieträger nur eine untergeordnete Rolle (zusammen etwa 13 %) spielen [2]. In den meisten Industrienationen dürfte die Verteilung ähnlich sein.
Der Prozesswärmebedarf ist dabei sehr heterogen: die benötigten Temperaturniveaus reichen von Niedertemperaturanwendungen wie etwa der Dampferzeugung bis hin zu Prozesstemperaturen von 1.500 °C und mehr, etwa in der Glasindustrie. Zudem geht es bei vielen industriellen Fertigungsprozessen oft nicht ausschließlich um das Erwärmen des Wärmguts, gleichzeitig spielen auch andere physikalische und chemische Prozesse wichtige Rollen, etwa beim Härten von Metallen, dem Schmelzen von Werkstoffen oder dem Brennen von Keramiken. Die Produkte reichen dabei von Lebensmitteln bis hin zu allgegenwärtigen Werkstoffen wie etwa Stahl, Aluminium, Glas, Zement oder Keramiken.
Prinzipiell existieren verschiedene Optionen, Prozesswärme zu dekarbonisieren, etwa die Abscheidung von CO2 aus dem Abgas und anschließende Speicherung oder Nutzung (CCUS: Carbon Capture, Utilization and Storage) oder der Einsatz von biogenen Brennstoffen wie Biomasse oder Biogas. Als am vielversprechendsten gelten jedoch momentan die Elektrifizierung (mit „grünem“ Strom, siehe z. B. [3]) und der Einsatz von Wasserstoff (H2). Während der Fokus bis vor einigen Jahren größtenteils auf einer weitestgehenden Elektrifizierung industrieller Fertigungsprozesse lag [3], [4], hat das Interesse an Wasserstoff als kohlenstofffreien Energieträger für die Prozesswärme in den letzten Jahren erheblich zugenommen [5].
Dies hat mehrere Gründe: zum einen ist es oft einfacher, einen komplexen erdgas-beheizten Fertigungsprozess auf einen anderen Brennstoff wie Wasserstoff umzurüsten als auf ein komplett neues Beheizungssystem wie eine resistive elektrische Heizung [6], [7]. Elektrische Öfen sind zudem oft in den übertragbaren Wärmemengen begrenzt, so dass sie oft größer ausfallen als vergleichbare gasbeheizte Aggregate [6], [8], [9], und es gibt Prozesse, die sich schwer oder überhaupt nicht elektrifizieren lassen, etwa in der Glas- oder Aluminiumindustrie [9], [10].
Wasserstoff ist auch aus einem anderen Grund interessant: Europa importiert heute knapp 60 % seines Energiebedarfs in Form von Kohle, Erdgas und Erdöl, und es ist absehbar, dass auch in Zukunft der Bedarf nicht allein durch erneuerbare Energien in Deutschland und Europa gedeckt werden wird [11], [12]. Ein globaler Energiehandel oder auch eine langfristige Speicherung großer Energiemengen wird auch in Zukunft notwendig sein, ist aber mit Hilfe von Strom im benötigten Maßstab aufgrund von Übertragungsverlusten und der niedrigen Energiedichte von Batterien nicht realisierbar. Wasserstoff bzw. Wasserstoff-Derivate wie etwa Ammoniak (NH3) sind hier eine der vielversprechendsten Optionen, dekarbonisierte Energie in großen Mengen interkontinental von Erzeugern (vor allem im globalen Süden) zu den großen Verbrauchern in Europa und Asien zu transportieren [12], [13] und saisonale Bedarfsschwankungen durch Speicher zu kompensieren. Untersuchungen zeigen, dass ein Großteil der existierenden, gut ausgebauten Erdgas-Infrastruktur mit vertretbarem Aufwand auf Wasserstoff umgerüstet werden kann [14], [15], was Wasserstoff gerade auch für energieintensive Hochtemperaturprozesse in der Industrie interessant macht, die aufgrund ihres meist kontinuierlichen Betriebs besonders auf die Versorgungssicherheit angewiesen sind.
Wasserstoff vs. Erdgas: Ein Vergleich der Verbrennungseigenschaften
Wasserstoff bietet als Brennstoff für Hochtemperaturprozesswärme eine Reihe von Vorteilen. Es muss jedoch berücksichtigt werden, dass es sich um einen chemisch völlig anderen Brennstoff handelt als Erdgas, mit sehr unterschiedlichen Eigenschaften. » Tabelle 1 veranschaulicht dies anhand einiger verbrennungstechnischer Angaben für Methan (CH4, stellvertretend für Erdgas), ein Gemisch aus 80 Vol.-% CH4 und 20 Vol.-% H2 sowie reinen Wasserstoff. Das CH4/H2-Gemisch wird hier berücksichtigt, da neben dem Aufbau eigener H2-Infrastrukturen wie etwa dem European Hydrogen Backbone [16] auch das direkte Einspeisen von Wasserstoff in bestehende Erdgasnetze in der Diskussion ist. Verschiedene Studien zeigen, dass gerade Gasgeräte aus dem häuslichen und gewerblichen Bereich, mit H2-Konzentrationen von bis zu 20 % Vol.-% sicher betrieben werden können [17], [18]. Aufgrund der Vielzahl der installierten Geräte (mehr als 200 Millionen in der EU [19]) gilt der Haushalts- und Gewerbesektor als besonders schutzwürdig. Allerdings ist die H2-Einspeisung in Erdgas nicht unumstritten [20].
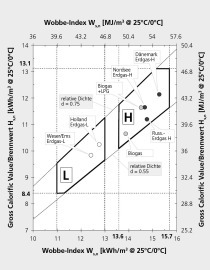
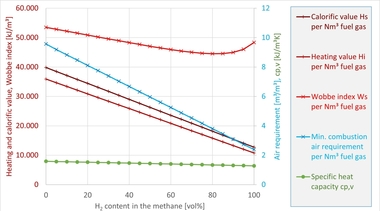
Anhand der Tabelle werden einige wesentliche Unterschiede zwischen den Brennstoffen deutlich. So ist beispielsweise der volumetrische Heizwert Hi,Vol von Wasserstoff ungefähr ein Drittel von dem von Erdgas bzw. Methan, gleichzeitig ist der minimale Luftbedarf Lmin von H2 ebenfalls deutlich niedriger. Dadurch verändern sich beim Brennstoffwechsel die Volumenströme von Brennstoff und Oxidator, mit denen der Verbrennungsprozess versorgt werden muss (gleiche Leistung und Luftzahl vorausgesetzt), wodurch sie die Strömung im Brennraum und ggfs. auch die Mischung von Brennstoff und Oxidator ändern. Dies kann Auswirkungen z. B. auf die Flammenform, die Wärmefreisetzung oder auch die Schadstoffemissionen, etwa im Hinblick auf Stickoxidemissionen (NOX) haben. Der (obere) Wobbe-Index WS sinkt ebenfalls bei höheren H2-Gehalten, allerdings deutlich moderater als Heizwert ode Luftbedarf. Der Wobbe-Index gilt in manchen Bereichen der Gastechnik als das zentrale Austauschbarkeitskriterium für gasförmige Brennstoffe [21], stößt aber gerade im Kontext der industriellen Verbrennung und beim Vergleich von Erdgas und Wasserstoff an seine Grenzen.
Von besonderer Bedeutung im Kontext der Verbrennung von H2 sind die adiabate Verbrennungstemperatur Tad und die laminare Verbrennungsgeschwindigkeit sL. Anhand von Tad wird deutlich, dass bei der Verbrennung von H2 mit deutlich höheren lokalen Temperaturen im Brennraum zu rechnen ist als bei der CH4-Verbrennung. Eine potenzielle Folge sind damit höhere NOX-Emissionen, da bei der Verbrennung von Gasen die NOX-Bildung hochgradig temperaturabhängig ist. Der Bildungspfad ist jedoch sowohl bei der Erdgasverbrennung als auch der H2-Verbrennung der gleiche, so dass sich viele bewährte Primärmaßnahmen zur NOX-Minderung für die Wasserstoffverbrennung anpassen lassen.
Einer der deutlichsten Unterschiede zwischen Erdgas und H2 findet sich in der laminaren Verbrennungsgeschwindigkeit sL, die großen Einfluss auf die Stabilisierung von Flammen hat. Für Wasserstoff ist sL bei stöchiometrischen Bedingungen um etwa den Faktor 5 größer als die Verbrennungsgeschwindigkeit von CH4..Die Auswirkungen auf die Verbrennung sind jedoch hochgradig technologieabhängig und vor allem für Vormischbrenner relevant, da hier die Gefahr eines Flammenrückschlags besteht. Solche Brenner sind z. B. in Gasheizungen im Haushalt oder auch bei Gasturbinen im Kraftwerkssektor zu finden. Bei den meisten Industriefeuerungen handelt es sich hingegen meist um nicht-vorgemischte Verbrennungsprozesse, wo ein Flammenrückschlag prinzipbedingt ausgeschlossen ist.
Vor dem Hintergrund der Dekarbonisierung spielen die bei der Verbrennung anfallenden CO2-Emissionen eine zentrale Rolle. Wird durch die Verbrennung von CH4 1 MJ an Wärme freigesetzt, werden dabei 55 g CO2 gebildet. Durch den Einsatz eines CH4/H2-Gemisches mit 20 Vol.-% H2 lassen sich die anfallenden CO2-Emissionen pro MJ um etwa 7 % reduzieren. Dies zeigt, dass eine teilweise Substitution von Erdgas durch H2 lediglich eine Zwischenlösung sein kann, für eine weitestgehende Dekarbonisierung ist der Einsatz von näherungsweise reinem H2 notwendig. Hierbei ist zudem die Herkunft des Wasserstoffs entscheidend, da beim Einsatz von konventionell mittels einer Dampfreformierung von Erdgas erzeugten H2 die Emissionen lediglich von der Feuerung hin zur Wasserstoffproduktion verlagert werden und letztendlich etwa 60 % mehr Treibhausgasemissionen anfallen, als wenn das Erdgas direkt verbrannt würde. Nur der Einsatz von H2, der mittels THG-armer Erzeugungspfade wie der Dampfreformierung + Carbon Capture and Storage („blauer“ Wasserstoff) oder der Wasser-Elektrolyse mit Strom aus erneuerbaren Quellen („grüner“ Wasserstoff) erzeugt wurde, stellt einen Beitrag zur Dekarbonisierung dar. Die in der Tabelle gegebenen spezifischen Emissionen beziehen sich jedoch ausschließlich auf die CO2-Emissionen, die durch die eigentliche Verbrennung selbst entstehen.
Welche Auswirkungen ein Brenngaswechsel hat, ist jedoch nicht nur von den Brenngasen selbst, sondern auch von der konkreten Anwendung und der eingesetzten Verbrennungstechnologie abhängig sind. So wird beispielsweise eine Gasheizung im häuslichen Bereich anders reagieren als eine industrielle Hochtemperatur-Thermoprozessanlage wie eine Glasschmelzwanne, ein Tunnelofen in der Ziegelindustrie oder eine Gasturbine im Kraftwerk. Auch die Anforderungen unterscheiden sich je nach konkreter Anwendung: während bei Gasgeräten im Haushalt der Fokus eher auf Kohlenmonoxid-Emissionen (CO) und der Flammenstabilität liegt, stehen bei großtechnischen Feuerungsprozessen meist Aspekte wie Produktqualität, energetische Effizienz und Stickoxid-Emissionen (NOX) im Vordergrund.
Wasserstoff für die Bereitstellung von (Hochtemperatur-)Prozesswärme
Neben Anwendungen in der Chemie-Industrie und dem Mobilitätsektor gilt Wasserstoff vor allem im Bereich der Hochtemperaturprozesswärme als interessante Dekarbonisierungsoption. Diese Prozesse zeichnen sich durch ein erhebliches Maß an Komplexität und Heterogenität aus, mit hohen Anforderungen an Produktqualität, Effizienz und Schadstoffemissionen.
Derzeit werden national und international zahlreiche Forschungsprojekte durchgeführt, in denen die Einsetzbarkeit von Wasserstoff für die Prozesswärmebereitstellung in energieintensiven Industrien untersucht werden. Ein Beispiel ist das vom Land Nordrhein-Westfalen geförderte „HyGlass“-Projekt [22], [23], das diese Fragestellungen im Kontext der Glasindustrie analysierte. Dabei lag der Fokus zum einen auf den Auswirkungen eines Wechsels von Erdgas auf Erdgas-Wasserstoff-Gemische und reinen Wasserstoff für typische Feuerungsprozesse in der Glasindustrie, zum anderen auf Aspekten der Produktqualität und der Versorgung mit Wasserstoff.
Die Glasindustrie zählt zu den energieintensiven Grundstoffindustrien, wobei der Großteil des Energiebedarfs (und somit auch der THG-Emissionen) auf den Schmelzprozess entfällt. Erdgas ist für die Branche der weitaus wichtigste Energieträger. Dies ist einer der Gründe, der Wasserstoff für die Glasindustrie interessant macht, da es oft einfacher ist, von einem gasförmigen Brennstoff auf einen anderen zu wechseln als zu einer völlig anderen Technologie wie etwa einer elektrischen Beheizung. Elektrisch beheizte Schmelzaggregate existieren zwar, sind jedoch in ihren Produktionsraten begrenzt, zudem gibt es u. U. Einschränkungen für bestimmte Glasprodukte und -qualitäten [9].
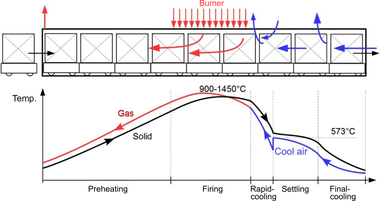
Im Rahmen des Projekts wurden u. a. die Auswirkungen des Brennstoffwechsels auf eine Underport-Feuerung, eine für regenerative Glasschmelzaggregate typische Brennerkonfiguration, an einem der Hochtemperatur-Brennerprüfstände des Gas- und Wärme-Instituts in Essen (GWI) untersucht (vgl. » Abbildung 1).
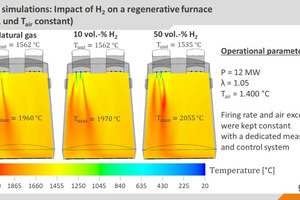
Dabei wurden die für eine regenerative Glasschmelzwanne typischen Randbedingungen, etwa Luftzahl (λ = 1,1), Luftvorwärmtemperatur (TLuft = 1.150 °C) und Ofentemperatur (ca. 1.600 °C), im Prüfstand bei einer Leistung von 500 kW nachgestellt. Reale Glasschmelzaggregate können Leistungen von bis zu 100 MW aufweisen. Im Rahmen der Experimente wurde der Verbrennungsprozess zuerst auf Erdgas als Referenz eingestellt, anschließend wurde der Wasserstoffanteil im Brenngas kontinuierlich erhöht. Brennerleistung, Luftzahl und Luftvorwärmtemperatur wurden dabei durch eine entsprechende Regelung konstant gehalten. » Abbildung 2 zeigt einen Blick in das Innere des Prüfstands für die verschiedenen Brenngasgemische.
Ein interessanter Effekt der H2-Beimischung ist, dass die Flamme mit höheren H2-Anteilen zunehmend transparenter wird, was mit den veränderten Strahlungseigenschaften zusammenhängt. Unter idealer Belichtung strahlt eine H2-Flamme zwar blass rötlich, aber unter normalen Bedingungen wirkt eine H2-Flamme mit bloßem Auge quasi unsichtbar, die Strahlung ist im Wesentlichen im Infrarot- und Ultraviolett-Bereich zu finden.
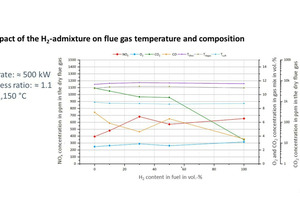
Im Rahmen der Untersuchungen wurden auch die Emissionen am Kamin aufgezeichnet, die in » Abbildung 3 zu sehen sind.
Bei den Untersuchungen wurde der Prozess so geregelt, dass trotz höherer H2-Konzentrationen die Luftzahl und die Ofenraumtemperatur konstant blieben. Das Diagramm zeigt erwartungsgemäß eine Reduktion der CO2-Konzentrationen mit höheren H2-Anteilen im Brenngas, aber auch einen Anstieg der NOX-Konzentrationen im Abgas. Dies ist auf die höheren lokalen Temperaturmaxima in der Reaktionsfront der Flamme bei der Beimischung von Wasserstoff zum Erdgas zurückzuführen. Da die Stickoxid-Bildung bei der Verbrennung von Gasen in der Regel vom thermischen Bildungspfad dominiert wird, führen höhere Temperaturen in der Flamme zur verstärkten NOX-Bildung, sofern ausreichend Sauerstoff vorhanden ist.
Allerdings sind „trocken“ gemessene NOX-Konzentrationen im Kontext der Wasserstoff-Verbrennung nicht das beste Kriterium, um Schadstoffemissionen zu bewerten, da diese Konzentrationen für das getrocknete Abgas bestimmt werden. Bei der H2-Verbrennung fallen jedoch deutlich höhere Konzentrationen an Wasserdampf an als bei der Erdgasverbrennung, so dass die Vergleichbarkeit der gemessenen Konzentrationen nicht mehr gegeben ist [24], [25]. So sind die gemessenen NOX-Konzentrationen bei der Verbrennung von reinem Wasserstoff bei gleichen Randbedingungen mehr als 60 % höher als bei der Verbrennung von Erdgas. Bezieht man die Emissionen jedoch auf die eingebrachte Energiemenge, also beispielsweise in der Einheit [mg/MJ], ergibt sich lediglich ein Anstieg der Emissionen von etwa 20 %. Zwar ist ein gewisser Anstieg der NOX-Emissionen beim Brennstoffwechsel von Erdgas auf Wasserstoff bei der Verbrennung mit (vorgewärmter) Luft physikalisch sinnvoll, aber die Analyse der „HyGlass“-Messungen zeigt, wie sehr die Vergleichbarkeit der Emissionen durch die Verwendung „trockener“ Konzentrationen verzerrt wird. Bei der in vielen Hochtemperatur-Anwendungen verbreiteten Oxy-Fuel-Verbrennung [26] kann der Wechsel zu Wasserstoff sogar zu deutlich reduzierten NOX-Emissionen führen, da das Erdgas als Stickstoffquelle entfällt, wie anhand von CFD-Simulationen [27] und Messungen nachgewiesen werden kann.
Für jeden industriellen Fertigungsprozess stellt die Produktqualität eines der wichtigsten Bewertungskriterien dar. Daher wurden im Rahmen von „HyGlass“ auch die Auswirkungen eines Wechsels von Erdgas auf Erdgas/Wasserstoff-Gemische und reinen Wasserstoff auf die Glasqualität in Zusammenarbeit mit der Hüttentechnischen Vereinigung der Deutschen Glasindustrie e.V. (HVG) untersucht.
Erwartungsgemäß hat die Veränderung des Brennstoffs Auswirkungen auf die Qualität des Produkts (vgl. auch » Abbildung 4), gerade bei einem sehr empfindlichen Produktionsprozess wie der Glasherstellung. Die Materialanalysen deuten darauf hin, dass der Wasserstoff im Brenngas oft nicht direkt mit dem Schmelzgut interagiert, dass es aber eine Reihe von indirekten Effekten gibt, die sich auf die Produktqualität auswirken können. So führt etwa der höhere Wasserdampfanteil in der Ofenatmosphäre, der sich aus der Wasserstoffverbrennung ergibt, dazu, dass Schwefel aus der Schmelze entzogen wird. Dieser Effekt war zu erwarten, da er beispielsweise auch beim Wechsel des Feuerungskonzepts von der Verbrennung mit regenerativ vorgewärmter Luft hin zur Oxy-Fuel-Verbrennung auftritt. Weitere Effekte sind die mögliche Reduzierung des O2-Gehalts in der Schmelze durch die Präsenz von CO und H2 im Ofenraum. Dies kann zu Verfärbungen im Glas führen [28].
Eine weitere Beobachtung der Versuche war, dass es bei bestimmten H2-Beimischraten zur verstärkten Rußbildung kam, wobei der Ruß zum Teil auch in den Glasproben nachgewiesen werden konnte [29]. Dies deckt sich mit Untersuchungen anderer Forschergruppen, die bei der Verbrennung von Erdgas-Wasserstoff-Gemischen ebenfalls höhere Ruß-Emissionen feststellen konnten [30], [31].
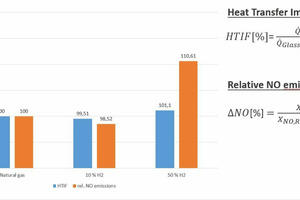
Mit Hilfe von CFD-Simulationen (CFD: computational fluid dynamics, dt. numerische Strömungssimulationen) wurden die Erkenntnisse der semi-industriellen Untersuchungen auf reale Industrieanlagen extrapoliert. Die Simulationen zeigen, dass die Auswirkungen des Brennstoffwechsel auf den Anlagenbetrieb verhältnismäßig gering sind, wenn die veränderten Brennstoffeigenschaften durch eine geeignete Verbrennungsregelung berücksichtigt werden, wie in den » Abbildungen 5 und 6 am Beispiel einer regenerativen 12 MW-Glasschmelzwanne zu sehen ist. Zwar ergeben sich im Ofenraum bei einer H2-Beimischung (10 und 50 Vol.-% H2 in Erdgas) lokal höhere Temperaturen als beim Betrieb mit Erdgas (und daraus resultierend auch eine verstärkte NOX-Bildung), die Auswirkungen auf die Wärmeflüsse in das Glasbad oder die globalen Temperaturverteilungen sind aber eher gering.
Die nur geringe Veränderung der Wärmeflüsse in das Glasbad (als Indikator für die energetische Effizienz und die Produktqualität im Prozess) im Vergleich zum Referenzfall mit Erdgas unterstreicht die Bedeutung entsprechender Mess- und Regelungstechnik, um die Auswirkungen der Brennstoffveränderung zu kompensieren. Die Veränderung der Wärmeflüsse in das Glasbad wird hier durch den so genannten Heat Transfer Impact Factor (HTIF) beschrieben, also als den Wärmefluss in das Glasbad für einen konkreten Fall, bezogen auf den Wärmefluss im Referenzfall, d. h. ein HTIF von 100 bedeutet, dass es keinerlei Veränderung im Wärmefluss gibt. Allerdings ist ein gewisser Anstieg der NOX-Konzentrationen aufgrund der höheren Maximaltemperaturen im System zu erwarten. Diese Anstiege sollten sich jedoch durch Anpassungen an den Verbrennungsprozessen beherrschen lassen.
Neben den eher technischen Aspekten wie Verbrennung, Glasqualität und Schadstoffbildung wurde im Rahmen des Projekts auch untersucht, inwieweit die Versorgung von Glasstandorten in Nordrhein-Westfalen durch lokal installierte Elektrolyseure mit Strom aus Wind- und Sonnenstrom realisiert werden kann. Mit Hilfe einer GIS-Analyse (GIS: Geographic Information System) wurden hierzu Glasstandorte in Nordrhein-Westfalen und ihre jeweiligen Energiebedarfe mit den Standorten und Erzeugungskapazitäten von Windturbinen und Photovoltaik-Anlagen in einem definierten Umkreis um die Glasproduktionsstätten in Verbindung gesetzt. Basierend auf der Annahme, dass die Windturbinen und PV-Anlagen im Umkreis ausschließlich für die Glashütten Strom produzieren, der mit einem Elektrolyseur in Wasserstoff umgewandelt wird, kann somit abgeschätzt werden, wieviel elektrolytisch erzeugter Wasserstoff lokal zur Beheizung der Glasschmelzaggregate potentiell bereitgestellt werden kann. Dabei wurden typische Laufzeiten und Elektrolyseur-Wirkungsgrade angenommen.
Die GIS-Analyse zeigt, dass selbst unter den genannten, sehr optimistischen Annahmen nur bei einem von neun Standorten eine vollständige lokale Eigenversorgung im Umkreis von 10 km realisiert werden kann, bei einem Umkreis von 20 km sind es lediglich drei Standorte. Diese Analyse unterstreicht die Bedeutung dekarbonisierter Energieversorgungsinfrastrukturen, insbesondere für energieintensive Industrien mit einem kontinuierlichen Energiebedarf.
Ammoniak als Brennstoff
Neben Wasserstoff als einem möglichen Brennstoff zur Dekarbonisierung von industriellen Feuerungsprozessen rückt in letzter Zeit immer mehr auch Ammoniak (NH3) in den Fokus des Interesses. Ammoniak wird in erster Linie als Wasserstoffträger gesehen, er bringt aufgrund seines höheren volumetrischen Heizwerts und vor allem seiner hohen Siedetemperatur (-33 °C bei Atmosphärendruck) erhebliche Vorteile im interkontinentalen Transport und der langfristigen Speicherung von Wasserstoff. So besagen Studien der International Energy Agency [32], dass ein erheblicher Anteil des global gehandelten Wasserstoffs in Zukunft wohl in Form von NH3 transportiert werden wird, ähnlich wie heute LNG (Liquefied Natural Gas). Während ein Großteil dieses NH3 an Land wieder in H2 und N2 aufgespalten werden wird, um den Wasserstoff dann in Wasserstoffnetze einzuspeisen, besteht auch die Möglichkeit, den Ammoniak direkt als Brennstoff einzusetzen. Dies wird zum einen für Schiffsantriebe diskutiert [33], [34], könnte aber auch für die Bereitstellung von Prozesswärme interessant sein, vor allem für Standorte, die (noch) nicht an eine dekarbonisierte Energieversorgungsinfrastruktur angeschlossen sind, aber dennoch ihre Prozesse dekarbonisieren wollen.
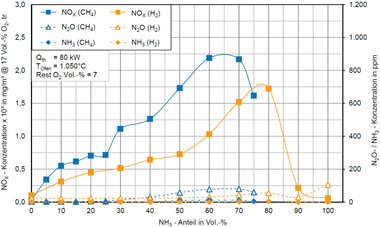
Ammoniak ist als Brennstoff nicht unproblematisch, wesentliche verbrennungstechnische Herausforderungen sind die hohe benötigte Zündenergie, der schmale zündfähige Bereich und die extrem niedrigen Verbrennungsgeschwindigkeiten, welche die Etablierung einer stabilen Verbrennung erschwert. Zudem besteht die Gefahr deutlich höherer Stickoxid-Emissionen, da durch den im Ammoniakmolekül enthaltenen Stickstoff andere NOX-Bildungsmechanismen, vor allem die NOX-Bildung über im Brennstoff gebundenen Stickstoff, relevanter werden als bei der Verbrennung von Erdgas oder Wasserstoff. Bisher gibt es kaum praktische Erfahrungen zum Einsatz von Ammoniak als Brennstoff im industriellen Maßstab, vor allem auch im Kontext der Prozesswärmebereitstellung. Daher analysiert das GWI derzeit in einer Reihe von Projekten (z. B. dem vor kurzem gestarteten Projekt „NH3-Ziegel“ [35]), wie NH3 als Brennstoff zur Dekarbonisierung von Prozesswärme in verschiedenen Branchen beitragen kann. Mit Hilfe von experimentellen Untersuchungen im Labor- und semi-industriellen Maßstab (bis zu 180 kW Brennerleistung) sowie reaktionskinetischen Simulationen wird betrachtet, wie Ammoniak sinnvoll und umweltfreundlich für die Bereitstellung von Prozesswärme eingesetzt werden kann.
» Abbildung 7 zeigt erste Ergebnisse dieser Arbeiten: an einem am GWI entwickelten nicht-vorgemischten Laborbrenner (Leistung 8 kW) wurde die Verbrennung von NH3/H2-Gemischen bei verschiedenen Drallzahlen S untersucht [36]. Da die Flammenstabilisierung bei der Ammoniakverbrennung aufgrund der Verbrennungseigenschaften von NH3 schwierig ist, wurde dem Brennstoff im Rahmen der Experimente zum einen Wasserstoff beigemischt, zum anderen wurde die Flammenstabilisierung durch eine Verdrallung der Luftströmung unterstützt. Die Abbildung zeigt, wie sich sowohl Drall als auch die H2-Beimischung auf die Flamme auswirken. Zudem wird deutlich, dass im Fall der reinen H2-Verbrennung die Flamme praktisch unsichtbar ist, jedoch selbst eine geringe Beimischung von NH3 zu erheblichen Änderungen im Strahlungsverhalten führt. Verantwortlich hierfür sind die NH2-Radikale, die sich bei der Oxidation von Ammoniak ergeben und der Flamme ihre charakteristische Farbe geben.
Zusammenfassung
Viele Industriebranchen, vor allem in den energieintensiven Grundstoffindustrien, stehen durch die Notwendigkeit der Dekarbonisierung ihrer Prozesse vor großen Herausforderungen. Ein Großteil der Treibhausgasemissionen in diesen Industrien wird durch die Verbrennung fossiler Brennstoffe zur Bereitstellung von Prozesswärme erzeugt. Neben der Elektrifizierung von Prozesswärme (vor allem im Bereich niedrigerer Prozesstemperaturen) stellt Wasserstoff aus regenerativen Quellen eine vielversprechende Option dar, um Prozesswärme, vor allem Hochtemperatur-Prozesswärme, klimafreundlich bereitzustellen.
Wasserstoff unterscheidet sich als Brennstoff deutlich von konventionellen Brennstoffen wie etwa Erdgas. Diese Eigenheiten der Wasserstoff-Verbrennung müssen beim Brennstoffwechsel in Thermoprozessanlagen berücksichtigt werden, um eventuelle negative Auswirkungen etwa im Hinblick auf Produktqualität oder Schadstoffemissionen zu minimieren. Einige dieser Effekte wurden anhand von Beispielen aus der Glasindustrie vorgestellt.
Auch Ammoniak kann eine interessante Option für die Dekarbonisierung von industriellen Fertigungsprozessen sein, vor allem für Standorte, die (noch) nicht an eine dekarbonisierte Energie-Infrastruktur angeschlossen sind. Ammoniak bringt jedoch auch besondere Anforderungen bzgl. der stabilen und schadstoffarmen Verbrennung mit sich. Entsprechende Forschungsprojekte zum Einsatz von NH3 für die Prozesswärmebereitstellung werden derzeit durchgeführt, auch am Gas- und Wärme-Institut Essen.